Structura moleculara a ... Ce substanță are o structură moleculară
După cum se știe, chimia studiază structura și proprietățilesubstanțe, precum și transformările lor reciproce. Un loc important în caracterizarea compușilor chimici este chestiunea particulelor din care fac parte. Pot fi atomi, ioni sau molecule. În solide intră în nodurile laturilor cristaline. Structura moleculară are un număr relativ mic de compuși într-o stare solidă, lichidă și gazoasă.
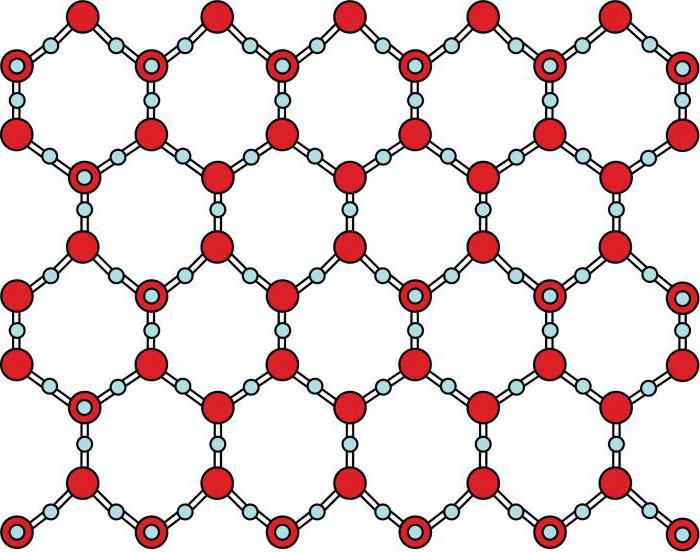
În acest articol vom da exemple de substanțe pentrucare sunt caracterizate de laturi de cristal molecular și, de asemenea, ia în considerare câteva tipuri de interacțiune intermoleculară, caracteristice pentru solide, lichide și gaze.
De ce trebuie să cunoașteți structura compușilor chimici
În fiecare domeniu al cunoașterii umane,pentru a distinge un grup de legi fundamentale pe care se bazează dezvoltarea ulterioară a științei. În chimie este teoria lui M.V. Lomonosov și J. Dalton, explicând structura moleculară atomică a materiei. După cum oamenii de știință au stabilit, cunoscând structura internă, putem prezice atât proprietățile fizice, cât și chimice ale compusului. Un număr mare de substanțe organice sintetizate artificial (materiale plastice, produse farmaceutice, pesticide etc.) au caracteristici și proprietăți predeterminate, cele mai valoroase pentru nevoile lor industriale și de uz casnic.

Cunoașterea caracteristicilor structurii și proprietățilorlegăturile sunt solicitate la efectuarea testelor de control, testelor și examinărilor într-un curs de chimie. De exemplu, în lista de substanțe propuse pentru a găsi răspunsurile corecte: ce substanță are o structură moleculară?
- Zinc.
- Oxid de magneziu.
- Un diamant.
- Naftalina.
Răspunsul corect este că: zincul are o structură moleculară, precum și naftalina.
Forțele de interacțiune intermoleculară
Sa stabilit experimental că molecula molecularăStructura este caracteristică substanțelor cu puncte de topire scăzute și duritate redusă. Cum putem explica instabilitatea laturilor cristaline ale acestor compuși? După cum sa dovedit, totul depinde de puterea influenței articulare a particulelor în nodurile lor. Are o natură electrică și se numește interacțiune intermoleculară sau forțe van der Waals, care se bazează pe influența moleculelor dipol încărcate opus unul asupra celuilalt. Sa dovedit că există mai multe mecanisme de formare a acestora, în funcție de natura substanței în sine.

Acizi ca compuși cu compoziție moleculară
Soluțiile majorității acizilor, atât organice,atât anorganice cât și anorganice, conțin particule polar, care sunt orientate unul față de celălalt prin poli cu încărcare opusă. De exemplu, într-o soluție de acid clorhidric HCI există dipoli, între care există interacțiuni orientale. Pe măsură ce crește temperatura moleculelor de acid clorhidric, bromhidric (HBr) și alți acizi cu conținut de halogen, efectul de orientare scade, deoarece mișcarea termică a particulelor interferează cu atracția lor reciprocă. În plus față de substanțele de mai sus, structura moleculară are zaharoză, naftalină, etanol și alți compuși organici.
Așa cum apar în particule încărcate induse
Anterior am considerat unul dintre mecanismele de acțiuneForțele Van der Waals, numite interacțiune orientare. În plus față de substanțele organice și acizii care conțin halogen, structura moleculară are hidrogen-apă. În substanțe constând din nepolar, dar predispus la formarea de dipoli, molecule, cum ar fi dioxid de carbon CO2, este posibil să se observe apariția particulelor încărcate induse - dipoli. Proprietatea lor cea mai importantă este capacitatea de a fi atrase unul de celălalt, datorită apariției forțelor de atracție electrostatică.
Structura moleculară a gazului
În subtitlul precedent am menționat acest lucrucompus, cum ar fi dioxidul de carbon. Fiecare dintre atomii săi creează în jurul său un câmp electric care polarizează atomul într-o moleculă de carbon din apropiere. Acesta este modificat într-un dipol, care, la rândul său, devine capabil de polarizare a altor particule de CO2. Ca rezultat, moleculele sunt atrase unul de altul. Interacțiunea inductivă poate fi observată și în substanțele formate din particule polare, deși în acest caz este mult mai slab decât forțele orientale van der Waals.

Dispersie interacțiune
Atât atomii cât și particulele care le compuncompoziția (electroni de bază) sunt capabile să o mișcare de rotație și vibrație continuă. Aceasta duce la apariția dipolilor. Conform studiilor mecanicii cuantice, apariția particulelor dvuzaryadnyh instantanee apare în solide și în fluidele sincronă, astfel încât capetele moleculelor aproape, apar cu poli opuși. Aceasta duce la atracția lor electrostatică, numită interacțiunea de dispersie. Este caracteristic tuturor substanțelor, cu excepția celor care se află în stare gazoasă, și ale căror molecule monoatomica. Cu toate acestea, forțele van der Waals pot apărea, de exemplu, la trecerea gazelor inerte (heliu, neon) în fază lichidă la temperaturi scăzute. Astfel, structura moleculară a fluidelor corporale sau determina capacitatea lor de a forma interacțiuni intermoleculare de diferite tipuri: orientarea indusă sau dispersie.
Ce este sublimarea?
Structura moleculara a corpului solid, cum ar fi cristale de iod, provoacă un fenomen fizic interesant ca sublimare - molecule volatilizare I2 sub formă de vapori violeți. Apare de pe suprafața unei substanțe în faza solidă, ocolind starea lichidă.
Această experiență eficientă din punct de vedere vizual este deseori efectuată înșcoli de chimie pentru a ilustra caracteristicile structurale ale grilelor cu cristale moleculare și proprietățile conexe ale compușilor. De obicei, este o duritate scăzută, puncte de topire scăzute și puncte de fierbere, căldură scăzută și conductivitate electrică, volatilitate.
Utilizarea practică a cunoștințelor despre structura substanțelor
După cum am văzut, între tipul de cristalinăstructura și proprietățile conexiunii pot stabili o anumită corelație. Prin urmare, dacă sunt cunoscute caracteristicile substanței, este suficient de ușor să se prezică caracteristicile structurii și compoziției particulelor: atomi, molecule sau ioni. Informațiile obținute pot fi, de asemenea, utile dacă, în sarcini de chimie, este necesar să se selecteze dintr-un grup definit de compuși substanțele având o structură moleculară, eliminând cele cu tipuri de laturi atomice sau ionice.

Rezumând, putem trage concluzia următoare: structura moleculară are un corp solid și structura sa spațială de laturi cristaline, iar particularitățile aranjamentului particulelor polarizate în lichide și gaze sunt complet responsabile de proprietățile fizice și chimice. Din punct de vedere teoretic de proprietăți ale compușilor care conțin dipoli, depinde de puterea interacțiunii intermoleculare. Cu cât polaritatea moleculelor și raza mai mică a atomilor în structura lor, cu atât mai puternică forțele de orientare generate între ele. In schimb, mai mulți atomi în moleculă, mai mare momentul său de dipol, și forțele, prin urmare, mai semnificative de dispersie. Astfel, structura moleculară a corpului solid și afectează mai mult pe forțele de interacțiune între particule - dipoli.